控制性减压通过 TREK-1 介导的细胞坏死和神经炎症的抑制减轻创伤性脑损伤后的压迫性损伤
由于脑损伤机制复杂且预后不良,创伤性脑损伤(TBI)被认为是最复杂的人类疾病之一。对于难治性颅内压(ICP)升高,去骨瓣减压术(DC)是降低创伤性颅内高压、改善预后的有效策略。然而,快速减压的标准程序与许多术后并发症有关,例如迟发性颅内血肿和弥漫性脑肿胀。之前的研究表明,控制性减压(CDC)手术可减轻脑损伤并降低 TBI 并发症的发生率。然而,潜在的分子机制尚未确定。
在中枢神经系统(CNS)中,多种细胞生理过程,包括神经递质释放、神经元兴奋性和可塑性,都受离子通道的调节,尤其是 Ca2+ 和 K+ 离子。弱内向整流的双孔K+ 通道-(TWIK-)相关的双孔K+ 通道(TREK)中的串联孔域属于最近发现的双孔K+(K2P)通道,包括6个亚家族的15个成员,负责维持神经元静息电位。
TREK-1,也称为 KCNK2 或 K2P2.1,在肺和大脑中高度表达。TREK-1 广泛存在于机体内,特别是在中枢神经系统中高表达,它的主要作用是控制细胞兴奋性并维持膜电位低于去极化阈值,因此参与调节多种生理和病理过程。它的激活受各种物理和化学刺激的调节,如机械拉伸、Gq 偶联组 I mGluRs 和 Gs 偶联 5-HR4 血清素受体。越来越多的证据表明,TREK-1 通道的功能障碍与多种神经病理学有关,包括抑郁、疼痛、癫痫和缺血。然而,TREK-1 在创伤性颅内高压疾病中的作用尚未完全确定。
在安徽医科大学附属医院神经外科的一项研究中,使用原代培养的皮质神经元的体外模型和大鼠体内创伤性颅内高压模型中研究了 CDC 对神经元创伤后压缩性损伤的影响,此外考虑到机械力对 TREK-1 激活的影响,还评估了 TREK-1 在 CDC 诱导的保护中的潜在作用。

皮质神经元 TNI 后压缩加重神经元损伤
为了在体外模拟 TBI 后的颅内高压,对原代培养的皮层神经元进行创伤性损伤和 0.5 MPa 压力处理 3 小时。H&E 染色结果显示,TNI 引起的神经元损失因压缩而显著增加(图1 a)。测量 LDH 释放以确定细胞毒性,TNI 诱导的皮质神经元中 LDH 释放的增加通过压缩得到增强(图1 b)。此外,通过测量 calcein AM 信号来测定神经元活力(图1 c)。结果表明,TNI 显著降低了皮层神经元中的钙黄绿素信号,而压缩进一步加剧了这种情况。
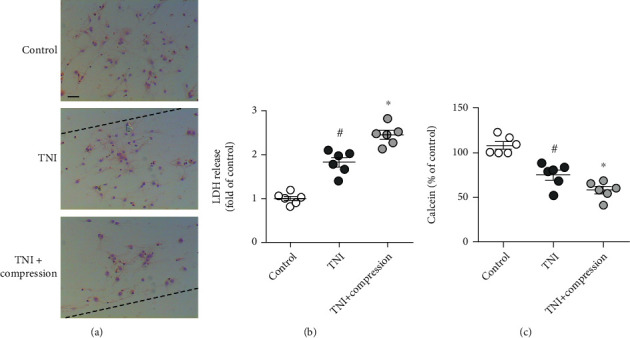
图1 压缩加重皮质神经元 TNI 后的神经元损伤。(a)H&E 染色的典型图片显示压缩会加重 TNI 后的神经元损失。(b)TNI 后压缩增加了 LDH 的释放。(c)TNI 后压缩降低了钙黄绿素信号。
CDC 减轻 TNI 后的压迫性损伤
为了模拟体外受控减压,0.5 MPa 压力在 1 小时(CDC 1h组)、2 小时(CDC 2h组)或 3 小时(CDC 3h组)内逐渐释放,一次完全释放作为对照。结果表明,CDC 2h和CDC 3h显著降低了TNI和压缩诱导的LDH释放,而CDC 1h没有效果(图2 a)。一致的是,CDC 2h 和 CDC 3h,但不是 CDC 1h,在 TNI 和压缩后明显增加了钙黄绿素信号(图2 b)。
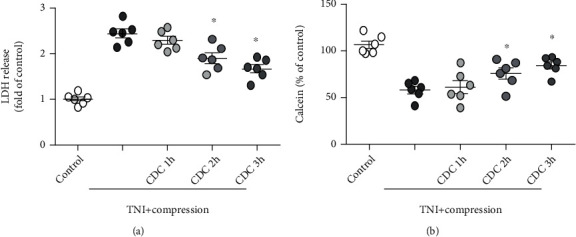
图2 CDC 减轻 TNI 后的压缩性损伤。(a)CDC 2h或 3h,但不是 1h,减弱了 TNI 后压缩引起的 LDH 释放增加。(b)CDC 2h或 3h,但不是 1h,减弱了 TNI 后压缩引起的钙黄绿素信号下降。
CDC通过 TREK-1 抑制皮质神经元中的Ca2+ 反应
为了研究 TREK-1 通道在 CDC 诱导的 TNI 后细胞内 Ca2+ 稳态调节中的作用,使用 TREK-1 阻滞剂 spadin 和 SID1900重复 Ca2+ 成像实验。结果表明,在TNI后,Spadin(1 μM,图3 a)和 SID1900(30 μM,图3 b)均能明显保存细胞内Ca2+ 浓度的降低。
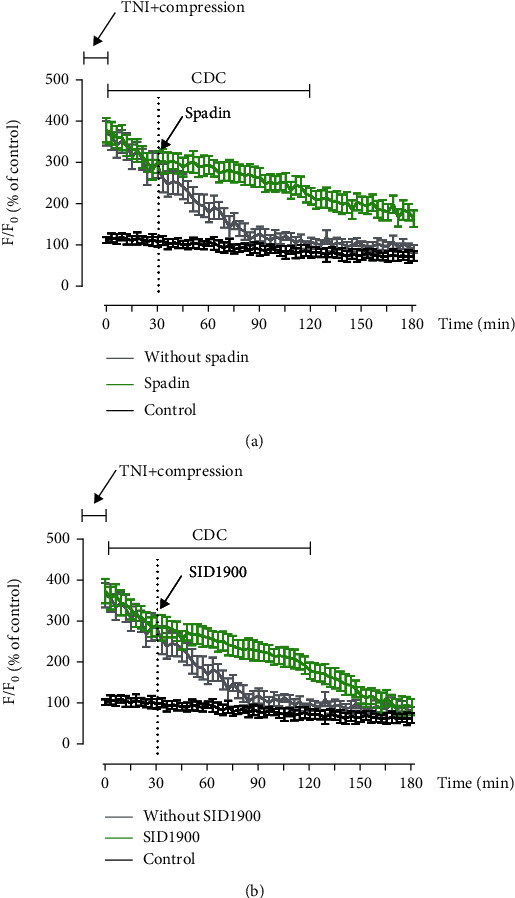
图3 CDC通过 TREK-1抑制 Ca2+ 反应。(a)Ca2+ 成像显示 CDC 诱导的细胞内 Ca2+ 过载衰减被 TREK-1 阻滞剂 spadin 消除。(b)Ca2+ 成像显示CDC 诱导的细胞内 Ca2+ 过载衰减被 TREK-1 阻滞剂 SID1900 消除。
CDC 减轻创伤性颅内高压后的脑损伤
为了在体内条件下证实上述发现,建立了大鼠创伤性颅内高压模型(图4 a)。脑含水量测定结果显示,与 RDC 组相比,CDC 20 分钟或 30 分钟,而非 CDC 10 分钟,显著减少脑水肿(图4 b)。神经学分析表明,与 RDC 相比,CDC 20 分钟或 30 分钟保留了运动功能,但 CDC 10 分钟没有(图4 c)。接下来,使用 NeuN 抗体进行免疫染色,以检测创伤性颅内高压后的神经元丢失(图4 d),结果表明,与 RDC 相比,CDC 20 分钟或 30 分钟,而不是 CDC 10 分钟,抑制神经元丢失(图4 e)。
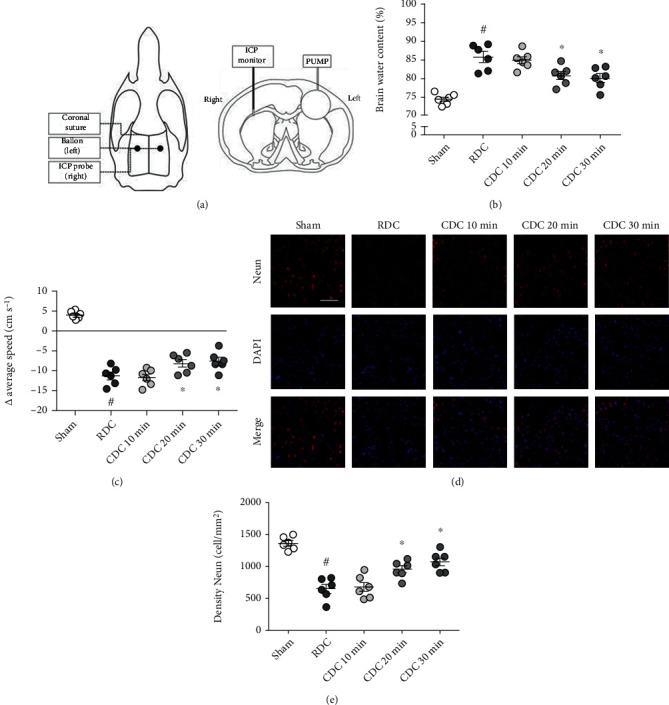
图4 CDC 减轻创伤性颅内高压后的脑损伤。(a)创伤性颅内高压模型的水平和冠状示意图。(b)脑水含量测定表明,与 RDC 相比,CDC 20 分钟或 30 分钟可减少脑水肿。(c)神经学分析表明,与 RDC 相比,CDC 20 分钟或 30 分钟可减轻运动障碍。(d、e)NeuN 染色和量化的典型图片显示,与 RDC 相比,CDC 20 分钟或 30 分钟可减少神经元损失。
CDC 减轻体内神经元坏死和神经炎症
为了研究 CDC 对创伤性颅内高压后神经元坏死性凋亡的影响,在脑切片上通过使用相应抗体的免疫染色来检测RIP1(图5 a)和 RIP3(图5 c)的表达。结果显示,与对照组相比,RDC 和 CDC 均增加了 RIP1 的表达,但这两组之间没有差异(图5 b)。然而,与 RDC 相比,CDC 显著降低了 RIP3 的表达(图5 d)。使用 CD68 抗体通过免疫染色确定小胶质细胞的活化(图5 e),结果显示 CDC 组小胶质细胞的激活低于RDC组(图5 f)。
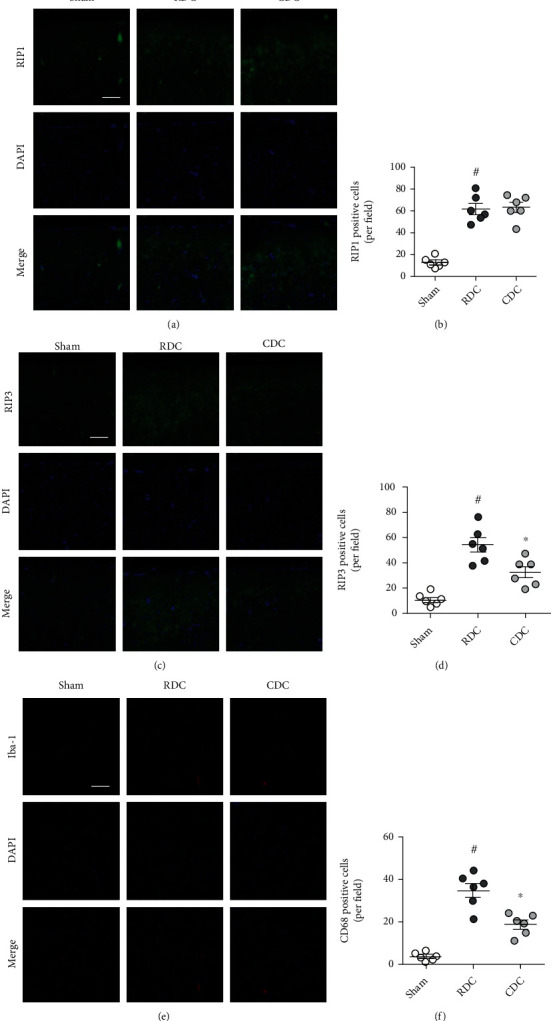
图5 CDC 减轻神经元坏死和神经炎症。(a、b)RIP1 染色和定量的典型图片显示 CDC 对 RDC 诱导的 RIP1 表达增加没有影响.(c、d)RIP3 染色和定量的典型图片显示,与 RDC 相比,CDC 减弱了 RIP3 的表达。(e、f)CD68 染色和量化的典型图片表明,与 RDC 相比,CDC 减弱了小胶质细胞的激活。
CDC 通过在体内激活 TREK-1 发挥神经保护作用
在创伤性颅内高压后的脑切片中使用 TREK-1 抗体进行了免疫染色(图6 a),结果显示,RDC 和 CDC 均增加 TREK-1 的表达,CDC 组 TREK-1 水平较高(图1 b)。通过与 NeuN 染色共定位,表明TREK-1 的表达增加主要在神经元中(图6 a)。为了进一步证实 TREK-1 在体内的参与,使用 spadin 和 SID9100 重复了脑含水量测定(图6 c)和神经功能测定(图6 d)。结果表明,spadin 和 SID9100 减弱了 CDC 对脑水肿和运动障碍的影响。
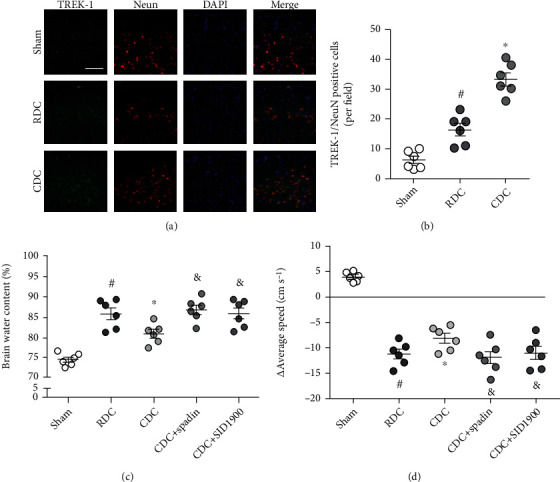
图6 CDC 通过在体内激活 TREK-1 发挥神经保护作用。(a、b)TREK-1 染色和定量的典型图片显示,与 RDC 相比,CDC 进一步增加了皮层神经元中 TREK-1 的表达。(c)脑水含量测定表明,spadin 和 SID1900 可防止 CDC 诱导的脑水肿抑制。(d)神经学分析表明,CDC 诱导的运动功能保留被 spadin 和 SID1900 逆转。
总之,目前的数据表明 CDC 在体外 2 小时或 3 小时和 CDC 在体内 20 分钟或 30 分钟发挥神经保护作用。潜在的潜在机制涉及 TREK-1 介导的细胞内 Ca2+ 稳态调节和神经元坏死性凋亡的抑制。
参考文献:Chen T, Qian X, Zhu J, Yang LK, Wang YH. Controlled Decompression Attenuates Compressive Injury following Traumatic Brain Injury via TREK-1-Mediated Inhibition of Necroptosis and Neuroinflammation. Oxid Med Cell Longev. 2021 Nov 8;2021:4280951. doi: 10.1155/2021/4280951. PMID: 34790287; PMCID: PMC8592713.
原文链接:https://pubmed-ncbi-nlm-nih-gov.proxy.library.carleton.ca/34790287/
图片来源:所有图片均来源于参考文献
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。
微信搜索公众号“Naturethink”,学习更多细胞压缩应力技术及应用!