人脂肪来源干细胞对间接共培养中隆突性皮肤纤维肉瘤细胞的影响
脂肪组织来源干细胞(ADSCs)可以从人皮下脂肪组织中大量提取,因此,它们是干细胞疗法最合适的细胞来源之一。ADSCs具有多向分化的能力,可以分化为多种细胞类型,如脂肪细胞、骨细胞、软骨细胞等。有报道称,在热/化疗过程中,装载生物材料作为抗肿瘤药物载体的ADSCs可选择性靶向实体肿瘤。这可以改善典型的药物递送方法,与磁共振成像跟踪诊断应用相关联。有趣的是,ADSCs也被证明表现出二元性。这些细胞不仅极大地促进了细胞再生,而且还促进了肿瘤的进展。ADSCs在促肿瘤特性上与肿瘤相关成纤维细胞(CAFs)相似,因此,ADSCs在肿瘤微环境(TME)内相互作用,促进癌细胞增殖、活力、侵袭性和化疗耐药性。
尽管关注ADSCs和肿瘤的研究越来越受到关注,但这些研究都没有检查ADSCs对隆突性皮肤纤维肉瘤(DFSP)的影响。DFSP是一种较为少见的低度恶性软组织真皮肿瘤,但属于最常见的皮肤肉瘤之一,起源于真皮内纤维组织细胞,可侵犯皮下组织,一般无包膜。肉瘤的发病机制不明确且多种多样,局部复发风险高,加上脂肪微环境(包括ADSCs和相关生长因子)信号传导的多变性,应进行更广泛的研究。
因此,考虑到脂肪、干细胞和分离的 ADSCs 在根治性肿瘤切除术后皮肤和软组织缺损中的使用越来越多,确定共定位 ADSCs 和 DFSP 细胞之间的可能相互作用对肿瘤安全性非常重要。不幸的是,关于这个问题的报告甚少。鉴于此,上海交通大学医学院附属第九人民医院整形外科的课题组团队首次进行了将原代DFSP细胞与ADSCs共培养的研究,随后,量化了增殖、迁移、侵袭和血管生成的变化,并将结果与DFSP细胞单一培养的结果进行了比较。此外,研究旨在从基因和蛋白质的角度进一步了解相互作用,如果ADSCs对DFSP细胞产生促进作用,它可能会提醒整形外科医生注意潜在的安全问题,因为这些ADSCs被注射到可能残留或休眠的DFSP细胞可以存活和发展的手术部位。具体内容发表在 Stem Cell Research & Therapy 期刊题为“Impact of human adipose tissue-derived stem cells on dermatofibrosarcoma protuberans cells in an indirect co-culture: an in vitro study”。

首先,通过成脂、成骨、成软骨分化实验检测ADSCs的多向分化潜能和干细胞标志物的表达水平。结果表明,从人脂肪组织中分离出的ADSCs表现出典型的ADSCs特征。
然后,采用CCK-8法评估ADSC-CM对DFSP细胞增殖的影响。结果表明,与对照组相比,ADSC-CM在第5天和第7天显著促进DFSP细胞的增殖。在前3天,实验组和对照组之间的细胞增殖率没有显著差异。
接下来,实验评估了ADSCs影响DFSP细胞迁移的能力。使用细胞划痕实验测试ADSC-CM影响DFSP细胞迁移的能力,其中DFSP细胞用ADSC-CM(实验性)、DMEM/F12 + 10%FBS(阳性对照)或DMEM/F12 SF(阴性对照)处理,结果表明,与阴性对照(DMEM/F12 SF)相比,ADSC-CM处理在6、12和24 h时显著促进了DFSP细胞的迁移(分别为1.71倍、2.01倍和3.56倍)。
然后,测试了基底室中ADSCs的存在是否可以诱导比Transwell系统中ADSC-CM产生的更强的反应(图1 B)。使用Transwell系统测试ADSCs对DFSP迁移细胞计数的影响,其中DFSP细胞与ADSCs(实验)、DMEM/F12+10%FBS(阳性对照)或DMEM/F12 SF(阴性对照)一起孵育(图1 A)。12 h时,阴性对照组有4.7±1.2个DFSP细胞迁移,而实验组有52.5±2.4个细胞迁移(图1 C)。24 h时,阴性对照组有6.2±2.2个细胞出现迁移,而实验组为38.2±12.6个细胞(图1 D)。这些结果表明,与阴性对照条件(DMEM/F12 SF)相比,ADSCs处理在12和24 h时间点更显著地促进了DFSP细胞的迁移(分别为11.17倍和6.16倍)。

图1 通过Transwell测定ADSCs对DFSP细胞迁移的影响。
(A)通过用结晶紫染色细胞来观察迁移的DFSP细胞。(B)不同条件下Transwell共培养系统的图示:将DFSP细胞接种到上腔室中,将DMEM/F12 + 10%FBS(阳性对照)、DMEM/F12 SF(阴性对照)或ADSC(实验性)加入下腔室,然后,在12和24小时测定细胞迁移。12 h(C)和24 h(D)时迁移的细胞数。
DFSP细胞的侵袭性使它们能够消化Matrigel 基质,该基质是从Engelbreth-Holm-Swarm肉瘤小鼠中分离出来的基底膜提取物。使用预先包被Matrigel 基质胶的Transwell系统测试ADSC-CM对DFSP侵袭细胞计数的影响,DFSP细胞用DMEM/F12+10%FBS(阳性对照)、DMEM/F12 SF(阴性对照)或ADSC-CM(实验性)处理(图2 A)。36 h时,阴性对照组有0.7±0.8个细胞侵袭下表面,而实验组有4.2±1.9个(图2 C)。这些结果表明,ADSC-CM处理在36 h时(7倍)比阴性对照组(DMEM/F12 SF)更显著地促进DFSP细胞的侵袭。
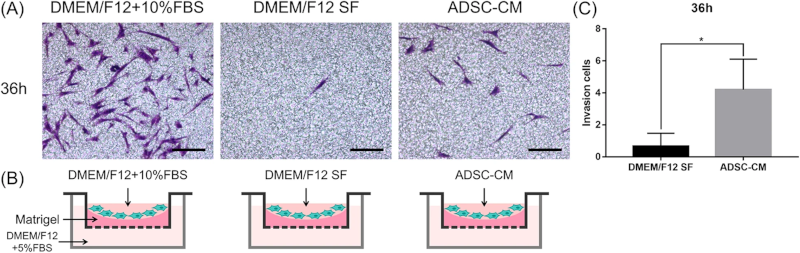
图2 ADSC-CM 对 DFSP 细胞侵袭的影响,通过预包被基质胶的 Transwell 测定。
(A)通过结晶紫染色来观察侵袭性DFSP细胞。(B)在不同条件下使用带有预包被基质胶的Transwell进行细胞侵袭测定的图示。将DFSP细胞加入DMEM/F12+10%FBS(阳性对照)、DMEM/F12 SF(阴性对照)或ADSC-CM(实验)接种到上腔室中,并将DMEM/F12+5%FBS加入下腔室。然后在 36 小时测定细胞侵袭。(C)36 小时时侵袭细胞的数量。
此外,为了评估ADSCs、DFSP细胞以及共培养的DFSP细胞和ADSCs分泌的蛋白质对血管生成的影响,将HUVECs与不同的CMs(ADSC-CM、DFSP-CM和共培养的DFSP/ADSC-CM)一起孵育,从而形成管状网络。孵育4小时后,实验观察到,与对照组(ADSC-CM或DFSP-CM)相比,与DFSP/ADSC-CM共培养的HUVECs形成的管状网络的网孔数、总管长和总分支长度显著增加,说明共培养的 DFSP/ADSC-CM增强体外血管生成能力。
最后,使用Transwell系统将ADSCs与DFSP细胞培养24 h后,DFSP细胞中PDGFRB和COL1A1的mRNA水平分别比单培养的DFSP细胞中的水平增加了1.4倍和1.5倍。48 h后,与单培养的DFSP细胞相比,共培养细胞中PDGFRB的蛋白水平适度升高,COL1A1蛋白水平显著升高。这说明,ADSCs增加了DFSP相关基因的表达和蛋白水平。
使用Transwell系统将ADSCs与DFSP细胞培养24 h后,DFSP细胞中促血管生成基因VEGF,HGF和bFGF的mRNA表达与单一培养的DFSP细胞相比分别升高1.32倍,1.2倍和1.4倍(图3 A-C)。48 h后,共培养(实验组)收集的上清液中VEGF、HGF和bFGF分泌水平显著高于单培养DFSP细胞(对照组)。实验组VEGF浓度为98.0±3.5 pg/mL,对照组为64.2±3.9 pg/mL(图3 D),实验组HGF浓度为287.4±14.1 pg/mL,对照组为202.5±12.0 pg/mL(图3 E),实验组bFGF浓度为31.6±6.3 pg/mL,对照组为19.6±1.8 pg/mL(图3 F)。这说明,ADSCs增加了DFSP细胞中生长因子基因的表达和共培养的DFSP微环境中生长因子的分泌。
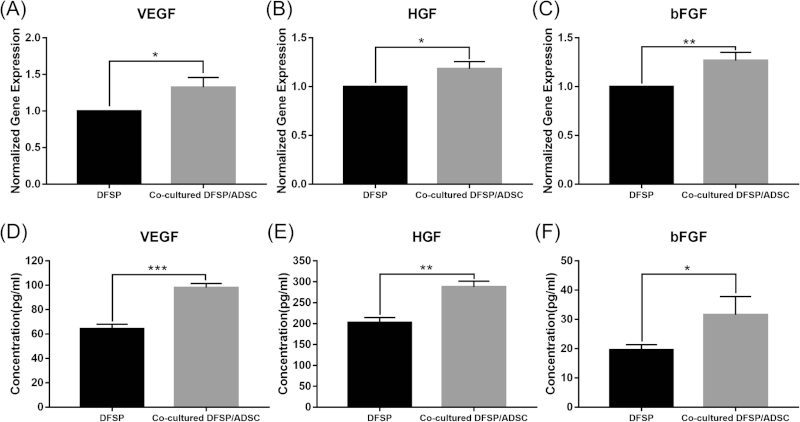
图3 ADSCs对DFSP细胞和微环境中生长因子基因表达和蛋白分泌的影响。
单培养组(对照组)或与ADSC共培养(实验组)的DFSP细胞中(A)血管内皮生长因子(VEGF)、(B)肝细胞生长因子(HGF)和(C)碱性成纤维细胞生长因子(bFGF)基因表达水平。ELISA法检测DFSP单培养组(对照组)和DFSP-ADSC共培养组(实验组)上清液48 h的(D)VEGF、(E)HGF、(F)BFGF的分泌水平。
总之,在该研究中,使用体外共培养模型探索了ADSCs和DFSP细胞之间的相互作用,以了解ADSCs对肿瘤发展的影响。该报告提供了ADSCs在体外显著影响DFSP细胞的多种恶性特征的证据,例如基因表达、蛋白质分泌、增殖、迁移、侵袭和血管生成。因此,如果在恶性肿瘤细胞附近给药,ADSCs可能会大大增加体内DFSP肿瘤发展的风险。在讨论基于ADSC的疗法对DFSP或残留DFSP细胞患者的安全性时,需要考虑该研究的结果。
参考文献:Yuan Z, Zhu Z, Zhu F, Ding F, Wang Y, Wang X, Luo X, Yang J, Liu F, Sun D. Impact of human adipose tissue-derived stem cells on dermatofibrosarcoma protuberans cells in an indirect co-culture: an in vitro study. Stem Cell Res Ther. 2021 Aug 6;12(1):440. doi: 10.1186/s13287-021-02512-5. PMID: 34362454; PMCID: PMC8344160.
原文链接:https://pubmed.ncbi.nlm.nih.gov/34362454/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。
点击了解
细胞流体剪切力|共培养|压力培养|牵张应变|血管培养|平行平板流动腔|仪器|上海泉众机电科技有限公司Naturethink
http://www.Naturethink.com/
Naturethink多细胞培养|共培养体系|共培养模型|共培养实验|动态细胞共培养|仿血流多细胞动态共培养系统
http://www.Naturethink.com/?product/81.html