将压缩力转化为癌症及其他疾病的细胞输出
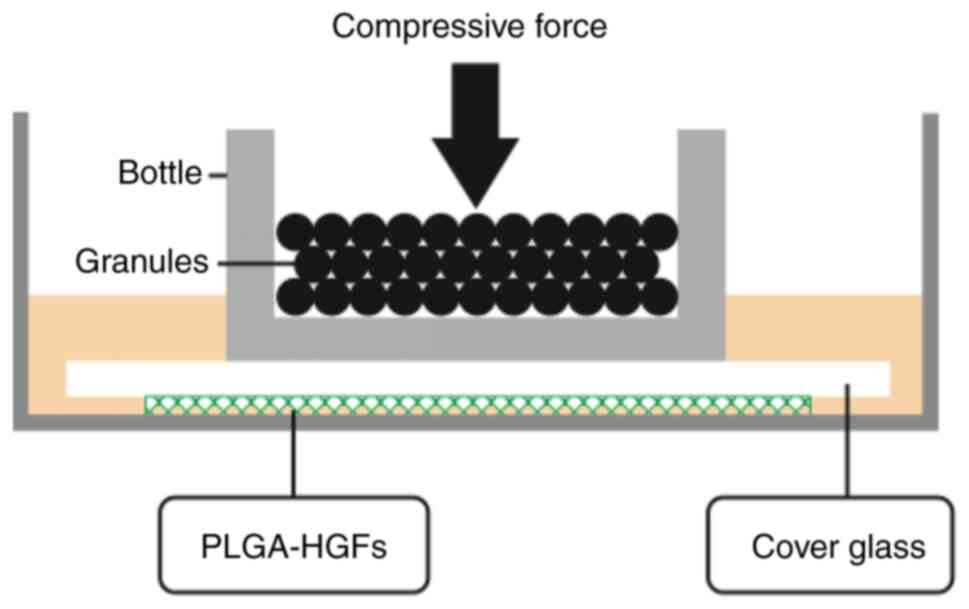
剪切力、拉伸力和压缩力是无处不在的对细胞产生生理反应的机械力。剪切力对应于施加平行于细胞表面的力,施加在细胞上的垂直的力并指向远离细胞表面的是拉伸力,垂直并指向细胞表面的是压缩力(图1 A)。机械力由机械传感器感知,机械传感器激活信号通路中的生化效应器,这个过程称为机械转导。其中,压缩力诱导的信号通路和细胞反应是迄今为止最不为人知的机制。为了在体外模拟压缩力对哺乳动物细胞在2D或3D环境中的应用,有不同的方法可用,这些方法在细胞和肿瘤生物学领域的应用正在扩大(图1 B-D)。下图回顾了机械负荷对细胞的影响(图1 B),由于亲水透明质酸在细胞外基质中的积累而引起的渗透和间质流体压力的变化(图1 C),以及在受限环境(如刚性基质)中的生长压力(图1 D、E),所有这些情况都模拟了体内环境。

图1 用于模拟 2D 和 3D 细胞培养物中体外压缩力产生的实验设计。
对压缩力的感知发生在细胞的不同位置(图2 A)。机械转导发生在质膜或肌动蛋白皮层中。细胞核变形同时或以顺序方式诱导生化通路,细胞质中的分子或细胞器拥挤参与对压缩力的感知。接下来,压缩力诱导不同的细胞输出,从细胞增殖到细胞死亡(图2 A-C)。直接施加压缩力可促进或减少细胞增殖、存活和分化,促进细胞骨架重塑、细胞运动和细胞迁移,控制细胞新陈代谢。所有这些细胞过程都参与了组织稳态。压缩力也通过自分泌或旁分泌信号起间接作用(图2 B、C)。
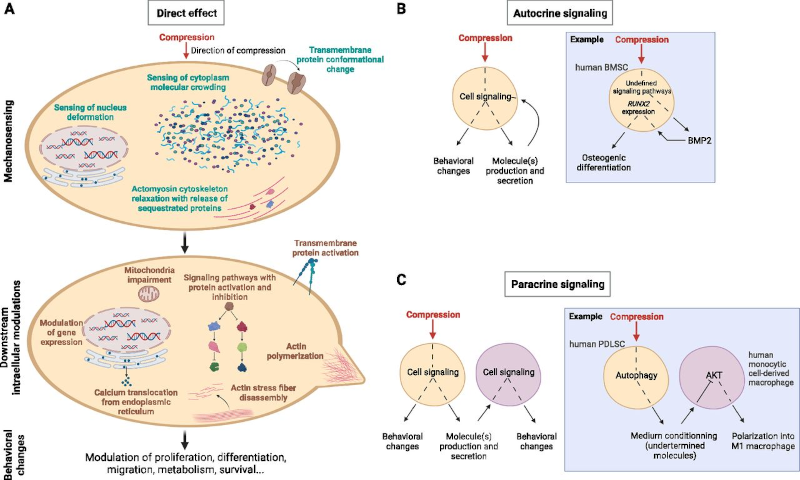
图2 人体细胞中压缩力机械转导的一般概述。
因此,物理压缩力控制着各种生物过程,但也与人类的病理有关。在某些情况下,过大的压缩力会导致病理变化。这是椎间盘退行性变的病例。在实体肿瘤发展过程中,肿瘤生长导致压缩力的产生,这种现象反过来改变了肿瘤和微环境细胞的行为。目前尚不清楚正常细胞、肿瘤细胞和肿瘤微环境细胞对压缩力的反应是否不同。
基于此,法国图卢兹第三大学、里昂高等师范学院生物科学系的研究员Céline Schmitter、Mickaël Di-Luoffo及Julie Guillermet-Guibert 在新的一篇研究综述中综合了细胞信号通路的压缩力在哺乳动物细胞中诱导细胞表型的途径,讨论了压缩了在健康和疾病中的重要性,还关注了癌症。具体内容发表在 Life Science Alliance 期刊题为“Transducing compressive forces into cellular outputs in cancer and beyond”。

组织稳态中由压缩调节的细胞输出
细胞环境决定了压缩是促进还是抑制细胞增殖。静态(即在规定的时间内施加一次)或循环(即以循环方式中施加)压缩力(在 10 kPa 范围内)以直接方式增加某些间充质细胞的增殖。增殖信号依赖于 RHOA 和 ROCK 信号,以及 BMP 信号和 SRC 诱导的 MAPK/ERK 通路。在对压缩力的反应中,由于单个信号节点的抑制不足以完全阻断压缩诱导的增殖,因此几个通路之间发生会相互作用。在大多数上皮细胞中,细胞增殖是由增加的机械张力触发的并被压缩力所抑制。压缩力诱导的细胞增殖阻断依赖于GSK-3β(糖原合酶激酶3β)和β-连环蛋白转录激活因子信号通路。
在骨重塑过程中,压缩力促进细胞分化。在转化生长因子 β3 存在下,长时间的动态压缩促进人滑膜来源的间充质干细胞的软骨分化。同样,长期的机械负荷增强了胶原微组织中人骨髓间充质干细胞的成骨分化。压缩促进间充质细胞的分化及其胶原基质的产生,这是一个参与骨愈合和重塑的过程。从机制上讲,不同的信号通路,例如PI3K / AKT的激活或MAPK / ERK信号的抑制,促进了骨髓间充质干细胞中压缩诱导的成骨分化。压缩力还通过参与骨再生的细胞类型之间的旁分泌调节触发细胞分化。循环压缩力,模拟骨愈合中的压缩作用,增强人骨髓间充质干细胞产生和分泌的BMP2,从而阻止其迁移。在稳态条件下,细胞分化需要对压缩力的主动响应。
压缩力诱导细胞信号传导,促进细胞骨架重组、细胞运动和迁移。在 HEK293 细胞中,压缩促进了对肌动蛋白细胞骨架重塑和细胞运动至关重要的 RHOA 和 ROCK 信号的激活。此外,支气管原代上皮细胞在受压时从非迁移性转变为迁移性表型。压缩促进参与迁移的关键细胞过程,例如板状伪足的形成和胶原基质培养的人骨髓间充质干细胞与细胞外基质的粘附。细胞骨架重排也是生理性高压缩力负荷的一种保护机制。
压缩力调节维持细胞行为的细胞新陈代谢。暴露于模拟其自然机械负荷的压缩力下原代人软骨细胞表现出特定代谢转录特征的上调或下调。这是一个重要的未来研究领域,因为肌动蛋白细胞骨架网络的解体发生在通过RHO和ROCK信号传导的压缩过程中,并可能导致糖酵解速率的降低。事实上,机械诱导的断裂的肌动蛋白促进糖酵解减少。
病理状态下的细胞压缩
压缩力与许多疾病有关。例如哮喘是一种慢性气道炎症疾病,其发展与对压缩力的感知有关;骨关节炎是一种以关节炎症为特征的疾病,压缩力控制骨关节炎的发生和进展;脑脊液在颅骨内长时间的高压力会导致颅内高压。
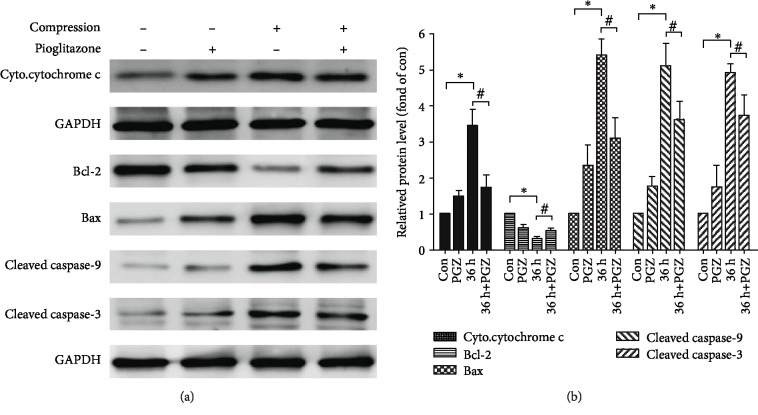
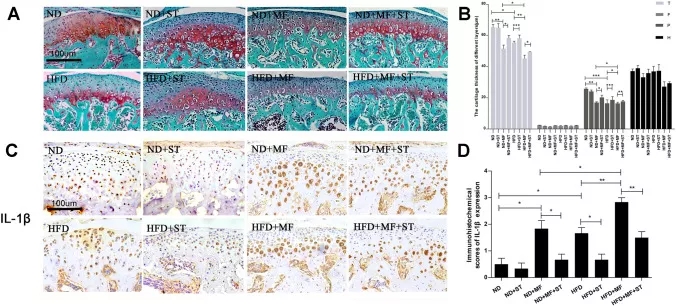
对导致病理的多步骤过程的研究强调了由过度压缩力引起的其他细胞输出。椎间盘退变(IVDD)是一种由椎间盘上不适当的机械负荷引起的病理,尤其会导致腰痛。椎间盘由软骨终板、纤维环和髓核(NP)三部分组成,其中NP 是维持结构稳态最重要的部分(图3 A)。由于过度压缩,NP基质蛋白的产生减少,导致无法维持基质稳态。这种损伤可以解释为:在机械负荷下,NP细胞中各种信号通路的激活通过诱导自噬、凋亡、坏死性凋亡或衰老来控制细胞存活/死亡平衡(图3 B)。压缩诱导的信号通路及其相互作用是未来工作的重点,旨在确定如何预防或减轻IVDD患者NP细胞的大量死亡。
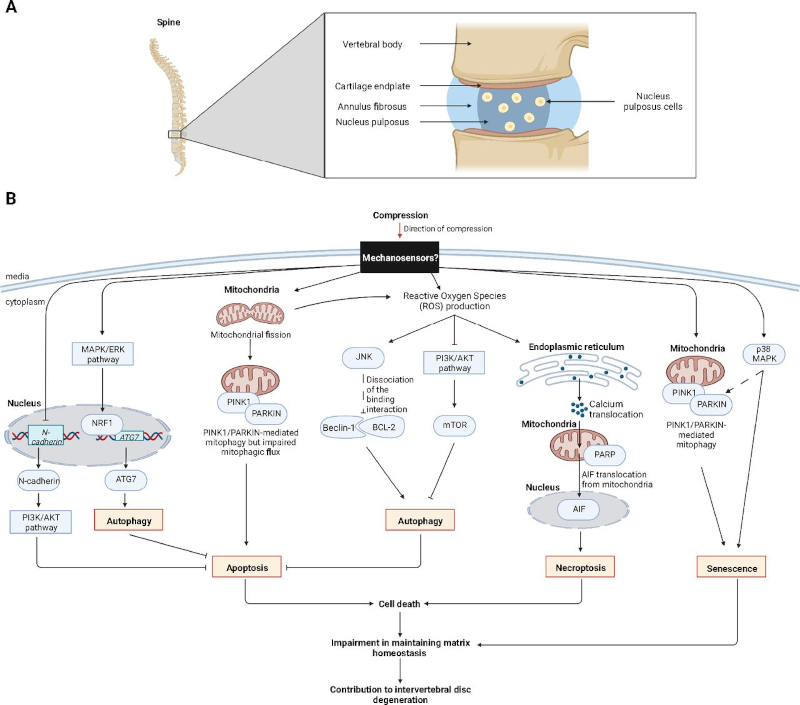
图3 压缩对髓核细胞信号传导和死亡相关细胞输出的影响。
肿瘤发展过程中的压缩——是促进还是抑制肿瘤的发生、进展或治疗反应?
与IVDD不同,肿瘤不是由压缩引起的,而是在实体肿瘤发展过程中压缩力增加,从而通过各种细胞修饰导致疾病进展(图4)。上皮细胞通过抑制细胞增殖、促进细胞死亡或挤压细胞来响应压缩,这是癌症发展早期阶段的保护机制(图4 A);然而,肿瘤上皮细胞适应了这种环境,随后的压缩导致肿瘤细胞增殖、迁移和存活增加(图4 B)。同样,压缩的微环境在早期阶段中阻止了肿瘤细胞增殖和肿瘤血管形成(图4 A),但在晚期加速细胞在恶劣环境中的增殖、迁移、存活(图4 C)。最后,肿瘤内压缩力的增加被邻近组织感知,加速肿瘤的发生(图4 D)。

图4 压缩力对癌症发生、进展和抑制的影响。
该图是对不同来源的癌细胞(A、B),如脑癌、乳腺癌和胰腺癌,以及癌症相关成纤维细胞(C)和癌症邻近组织(D)进行的体外和体内研究的总结。
总之,了解选择性压缩力诱导的肿瘤效应对于肿瘤机械疗法的成功是必要的,例如靶向基质传感或形态发生程序的肿瘤治疗。预估患者的压缩力对于更多地了解癌症的机械生物学并为每位患者量身定制机械疗法是必要的。减轻或增加患者治疗的肿瘤压力仍然是一个有争议的问题。然而,随着压缩力激活选择性致癌途径,压缩可能会诱导新的肿瘤脆弱性,这可以通过新兴的机械疗法来靶向。
参考文献:Schmitter C, Di-Luoffo M, Guillermet-Guibert J. Transducing compressive forces into cellular outputs in cancer and beyond. Life Sci Alliance. 2023 Jun 26;6(9):e202201862. doi: 10.26508/lsa.202201862. PMID: 37364915; PMCID: PMC10292664.
原文链接:https://pubmed.ncbi.nlm.nih.gov/37364915/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。
点击了解
细胞流体剪切力|共培养|压力培养|牵张应变|血管培养|平行平板流动腔|仪器|上海泉众机电科技有限公司Naturethink
http://www.naturethink.com/
Naturethink压力培养|压力刺激|压应力|机械压应力|细胞压力加载|细胞体外加力系统|细胞低压力、细胞正压力|仿生压力细胞培养仪
http://www.naturethink.com/?product/61.html