运动通过 STAT3 促进骨生成来维持骨稳态
运动介导的机械力在维持骨稳态方面起着至关重要的作用,缺乏运动会加速骨量流失,使骨骼减少,骨质减弱,从而降低骨骼的强度和结构。因此,阐明运动介导的骨稳态的潜在机制将是治疗由缺乏运动引起的骨质疏松症的关键因素。
骨稳态是通过成骨细胞介导的骨形成和破骨细胞介诱导的骨吸收之间的平衡来维持的,不平衡会导致骨骼功能障碍和骨骼不完整。据报道,机械负荷促进骨形成。成骨细胞作为骨形成细胞,来源于骨髓间充质干细胞(BMSCs),可以将机械信号转化为生物信号,协调骨吸收和形成。然而,BMSCs调节运动驱动骨形成的潜在分子机制仍未明确。
信号转导和转录活化因子3(Stat3)是在多种细胞中普遍表达的细胞质转录因子,可能成为机械转导各个方面的重要介质。先前的研究表明,STAT3 对骨骼生长和骨稳态至关重要,并且可能是调节骨稳态的潜在机械敏感分子靶点。
因此,上海交通大学医学院附属第九人民医院口腔颅颌面科课题组的一项研究旨在集中探讨了 STAT3 如何在运动介导的机械力下调节骨稳态。该研究采用跑轮模型和悬尾模型研究了骨代谢和STAT3在运动前后中的作用,揭示了STAT3 可能作为缺乏运动引起的骨质疏松症的潜在靶点。具体内容发表在 International Journal of Biological Sciences 期刊题为“Exercise maintains bone homeostasis by promoting osteogenesis through STAT3”。

首先,研究人员建立了一个跑轮模型来研究运动下的骨骼变化和骨代谢(图1 A)。H&E染色显示运动后骨小梁骨量增加(图1 B)。与对照组相比,运动组小梁骨量增加(图1 C),皮质骨厚度没有明显变化(图1 D)。骨量增加可能是由于骨形成增加、骨吸收减少或两者兼而有之。与对照组相比,运动组的矿物质沉积率(MAR)更高(图1 E)。TRAP染色表明运动组小鼠表现出增加的骨形成,破骨细胞也更多,且骨吸收也增加。这些结果表明,机械力通过增加骨形成诱导体内骨量增加。
先前的研究表明,STAT3在骨代谢中起着重要作用,因此实验研究了STAT3在运动中是否可能发挥同样的作用。运动小鼠中p-STAT3+ OPN+ 细胞数量的增加(图1 F)暗示了运动介导的骨量增加可能与STAT3活性密切相关。
为了进一步研究运动与 STAT3 活性之间的关系,利用小鼠尾部悬吊(TS)模型来模拟运动损失(图1 G)。H&E染色显示TS组运动损失后骨量减少(图1 H)。同时,BV/TV、Tb.N.和 Ct.Th 显著下降(图1 J)。此外,运动损失降低了TS小鼠的MAR,这表明运动损失抑制了骨形成(图1 K)。TRAP染色显示,运动损失增加了TS小鼠的破骨细胞数量,表明运动损失增加了骨吸收。此外,在运动损失小鼠的股骨中观察到p-STAT3+ OPN+ 细胞的减少(图1 L)。

图1 成骨细胞STAT3与体内运动介导的机械力密切相关。
为了进一步研究机械力是否可以激活STAT3,应用张力系统在体外模拟循环机械拉伸应变(CMS,10%,0.5 Hz,8 h )。CMS后,BMSCs显示ALP活性增加,成骨特异性标志物表达水平升高(图2 A、B)。p-STAT3在BMSCs中的表达显著增加(图2 C)。这与p-STAT3阳性BMSCs的数量显著增加一致(图2 D)。CMS后BMSCs中STAT3阳性表达从细胞质转移到细胞核(图2 E)。这些结果表明,成骨细胞STAT3活性可能与运动诱导的骨形成和骨量密切相关。
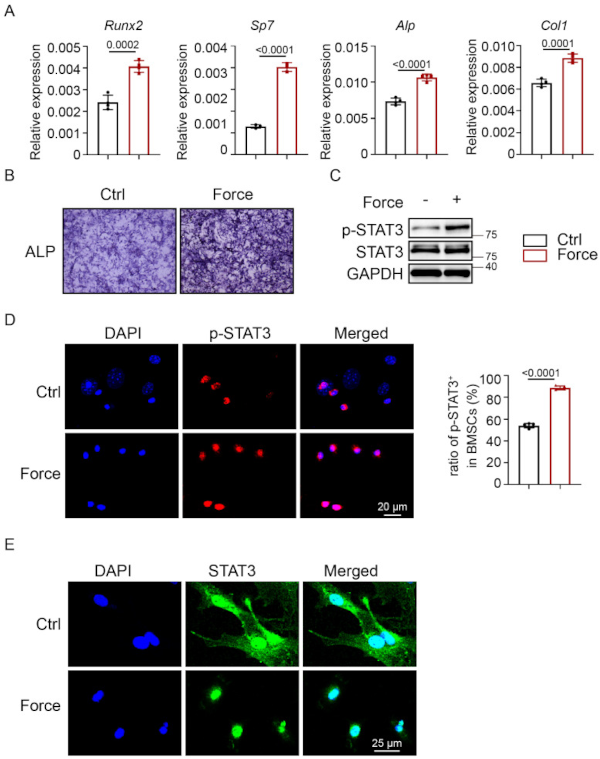
图2 体外机械力激活成骨细胞STAT3。
由于 STAT3 被认为是一个有前途的抗癌靶点,研究人员探讨了 STAT3 的药理学抑制是否可以调节运动介导的骨形成。首先,在有和没有JAK2-STAT3抑制剂AG490 下于CMS中培养BMSCs,结果表明,在AG490处理下,无论是否有CMS,STAT3的磷酸化都被显著抑制,ALP活性降低,成骨特异性标志物表达水平降低。
在小鼠腹腔内注射AG490后,发现运动小鼠存在骨质流失,骨量减少,且MAR受损,表明运动小鼠的骨形成活性在AG490处理后减弱。TRAP染色显示AG490处理的运动小鼠的破骨细胞数量较少,骨吸收减少。这些结果说明,STAT3 的药理学抑制可以减缓骨骼发育并中断机械力介导的骨稳态,表明 STAT3 可能是机械力介导的疾病的合适靶点。
接下来,为了进一步探讨STAT3对机械力暴露的BMSCs成骨细胞分化的影响,用表达GFP(Ad-EGFP)和CRE重组酶(Ad-CRE)的腺病毒感染Stat3fl/fl小鼠BMSCs 以敲除STAT3(图3 A)。CMS后,Ad-CRE组的ALP活性降低(图3 B)。成骨标志物的mRNA表达与ALP染色一致(图3 C)。
然后应用他莫昔芬诱导成骨细胞系表达cre、Col1ERT2 cre 来诱导运动期间Stat3 的敲除(图3 D、F)。与AG490处理的小鼠一致,与Stat3fl/fl 相比,无论运动还是不运动,Stat3Col1ERT2小鼠的小梁骨量均显著减少(图3 G-H)。此外,在对照组和运动组中,Stat3Col1ERT2小鼠没有差异,这表明成骨细胞STAT3在机械力作用下的重要作用。Stat3Col1ERT2小鼠的MAR降低,表明在缺乏STAT3的情况下,骨形成活性被消除(图3 I),且破骨细胞较少,表明在缺乏STAT3的情况下,骨吸收活性下降。这些结果表明,机械敏感的STAT3在运动介导的骨形成过程中起着至关重要的作用。
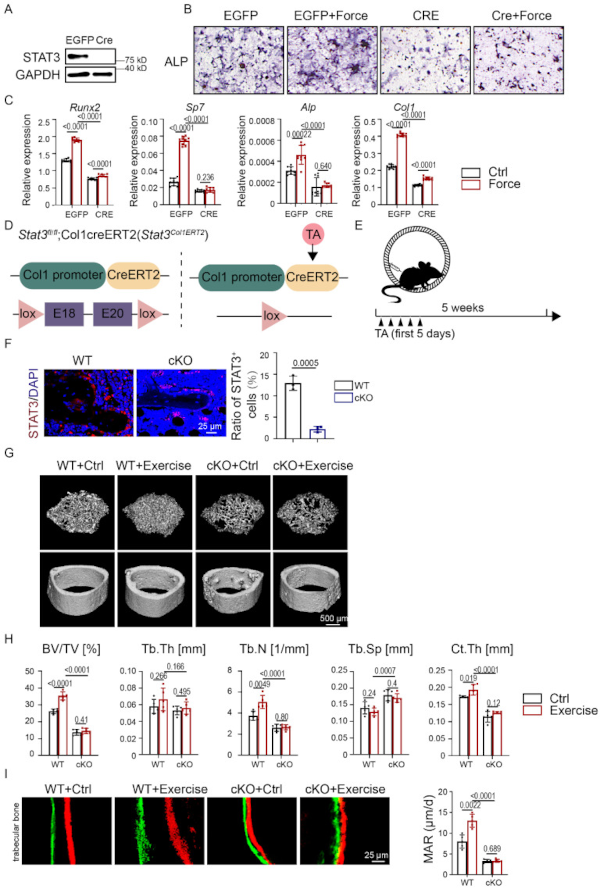
图3 体外和体内机械力作用下,成骨细胞谱系特异性缺失STAT3会损害骨形成。
由于机械力可以促进STAT3磷酸化,因此实验认为STAT3的激活可以在没有机械力的情况下促进成骨细胞分化并维持骨稳态。为了验证这一假设,首先分析了用 STAT3 激动剂 colivelin 处理的 BMSCs 中 p-STAT3 的蛋白水平,结果表明,colivelin 处理导致 p-STAT3 水平更高,发现colivelin促进成骨分化,成骨标志物表达也有所提高。
为了进一步研究colivelin是否可以在没有运动的情况下维持骨稳态,建立了TS模型(图4 A)。与TS小鼠相比,colivelin处理的TS小鼠小梁骨的BV/TV和Tb.N. 显著升高(图4 B、C),这意味着colivelin可以相对挽救骨质流失,且MAR增加,表明colivelin在运动损失下促进骨形成(图4 D)。这些结果充分说明,STAT3的药理激活可用于预防因运动缺失引起的骨质疏松症。
最后,实验试图检测废用性骨质疏松后colivelin的治疗效果(图4 F)。结果表明,骨质流失后colivelin增加骨小梁骨BV/TV和Tb.N.,表明STAT3的激活加速了骨质流失的恢复速度(图4 G、H)。钙黄绿素-茜素红双标记提示colivelin促进骨形成(图4 I)。这些数据都表明,STAT3可能作为治疗废用性骨质疏松的合适药理学靶点。

图4 STAT3的药理激活在体内无机械力的情况下促进骨形成。
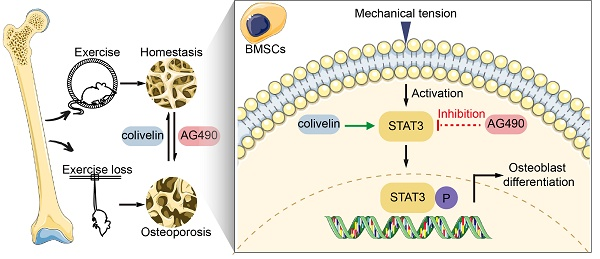
图5 图形概要
目前的研究表明,STAT3 在体内和体外均可作为骨稳态的机械转导调节因子。STAT3 的药理学抑制和成骨细胞谱系特异性消除可通过减少骨形成来中断机械力介导的骨稳态。同时,STAT3的药理激活促进了成骨细胞分化,并在缺乏运动的情况下挽救了骨质流失。总之,该研究明确了 STAT3 在运动介导的骨形成中的关键作用,并揭示了STAT3可能作为未来治疗骨代谢性疾病的合适药理学靶点。
参考文献:Huang X, Zhu Y, Sun S, Gao X, Yang Y, Xu H, Jin A, Liu Y, Jia H, Dai Q, Jiang L. Exercise maintains bone homeostasis by promoting osteogenesis through STAT3. Int J Biol Sci. 2023 Apr 2;19(7):2021-2033. doi: 10.7150/ijbs.82744. PMID: 37151888; PMCID: PMC10158023.
原文链接:https://pubmed.ncbi.nlm.nih.gov/37151888/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。
点击了解
细胞流体剪切力|共培养|压力培养|牵张应变|血管培养|平行平板流动腔|仪器|上海泉众机电科技有限公司Naturethink
http://www.naturethink.com/
Naturethink牵张力|拉伸力|细胞拉伸|细胞牵张|细胞牵张应变|牵张应变细胞培养仪
http://www.naturethink.com/?product/19.html