结肠癌细胞和肿瘤相关成纤维细胞的共培养可概括间充质型结肠癌的侵袭性特征
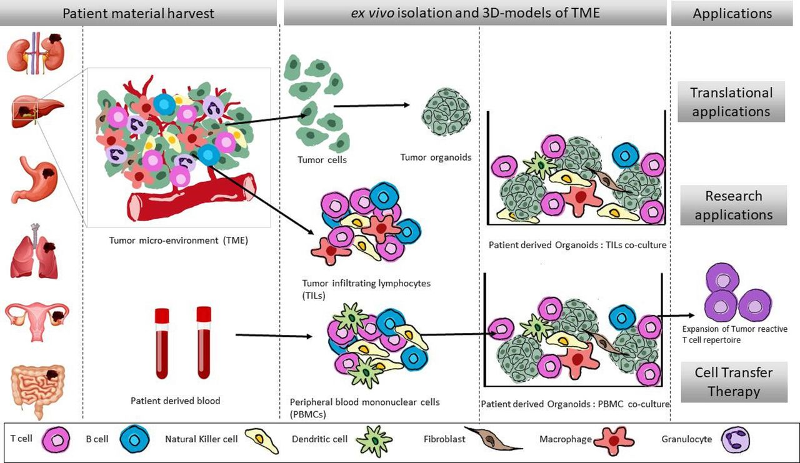
结肠癌是成人癌症相关死亡的主要原因之一。微卫星不稳定性(MSI)、KRAS 或 BRAF基因中存在激活突变和/或 T 细胞浸润等特征均显示与预后和/或治疗反应相关。免疫治疗的成功取决于免疫细胞对肿瘤的浸润以及来自影响免疫细胞分化和功能的肿瘤微环境(TME)的信号。TME 由细胞外基质(ECM)成分、内皮细胞、免疫细胞和肿瘤相关成纤维细胞(CAFs)组成,在确定肿瘤免疫细胞功能方面发挥重要作用。特别是CAFs,促进了结肠癌的发生,进展,转移形成和治疗耐药性。当被肿瘤细胞激活时,CAFs 可能反过来促进肿瘤细胞的侵袭性行为。此外,CAFs 有助于免疫抑制性 TME 的产生。从功能上讲,细胞外基质(ECM)成分的持续沉积是 CAF 介导的关键特征,可影响侵袭性肿瘤细胞行为和免疫抑制的多个方面。
在结肠癌中,“间充质型”共识分子亚型4(CMS4)的特征是 CAF 含量高和反映血管生成、炎症和免疫抑制的基因表达程序。尽管 CMS4 MSI-L 结肠癌具有免疫抑制性质,但已从此类肿瘤中分离出肿瘤特异性新抗原反应性 T 细胞。因此,提高 CMS4 结肠癌中肿瘤反应性 T 细胞的活性可能是一种很有前景的治疗策略。新型治疗策略的设计和测试需要用于研究CMS4(富含CAF)结肠癌的模型系统。为了揭示肿瘤细胞和CAFs之间的相互作用如何决定肿瘤行为,需要基于类器官的模型系统,其中两种细胞类型以可重复和稳健的方式共培养。
在荷兰乌得勒支大学医学中心以及鹿特丹伊拉斯谟大学医学中心研究课题组的一项实验中,该团队提出了结肠癌类器官和CAFs在高度标准化的无血清培养基和优化的ECM中的长期共培养模型。在这些条件下,肿瘤细胞和CAFs自发地组织成上层结构,同时使ECM变硬和收缩。上皮腺结构与CAF轨道直接接触,与患者结肠肿瘤的组织学非常相似。单细胞转录组学分析进一步证明了共培养诱导的临床相关肿瘤细胞和 CAF 表型的产生。两种细胞类型都需要产生抑制T细胞增殖的免疫抑制环境。具体内容发表在 Frontiers in Immunology 期刊题为“Co-cultures of colon cancer cells and cancer-associated fibroblasts recapitulate the aggressive features of mesenchymal-like colon cancer”。

在共培养模型中,首先将小类器官接种在含有基质胶和胶原蛋白I 的共培养基质中,然后在共培养基中加入CAFs(图1A)。在最初的2-3天内,CAFs在含有类器官的基质液滴周围组织成一个连续的圆圈(图1 B、C)。在液滴内,CAFs组织成基质轨迹,同时,类器官沿着这些CAFs轨迹重组。最终,所有单独的类器官融合成一个围绕 CAF 轨道的单个实体 (图1 D),形成肉眼可见的“微型肿瘤”(图1 E)。这些数据表明,在优化条件下与肿瘤细胞共培养CAFs会导致自发的ECM重组和类似肿瘤组织的上层结构的组装。目前尚不清楚是什么原因导致了细胞重组。

图1 肿瘤细胞和CAFs自发重组成宏观微型肿瘤。
接下来,实验旨在从机制上深入了解 CAFs 和肿瘤细胞如何相互影响彼此的表型以诱导 ECM 重塑和细胞重组。为此,通过FACS分选对单培养(CAF-2d、CAF-3d、类器官)和共培养(CAF/类器官)分离的两种细胞类型进行了单细胞RNA测序。总共分析了 949 个细胞,确定了3 个肿瘤细胞群(clusters 1-3)和 3 个CAF 群(clusters 4-6)。肿瘤细胞与 CAFs 共培养导致 cluster-2 细胞减少,而 cluster-3 细胞强烈扩增。为了深入了解不同肿瘤细胞群和CAFs之间的表型差异,进行了差异基因表达分析。Cluster-1 肿瘤细胞的特征是缺氧和糖酵解相关基因的表达,Cluster-2由95%的单培养肿瘤细胞组成,增殖相关基因表达最高,Cluster-3 肿瘤细胞主要由共培养的肿瘤细胞组成,上皮基因(KRT19、EPCAM、CDH1)表达较低,间充质基因(SPARC、TIMP1、VIM、MMP2)和基因集(Hallmark EMT)表达较高,反映了(部分)上皮间充质转化 (EMT)。此外,CMS4 识别基因集(CMS2 RF)(主要由 CAF 表达的基因组成)在 Cluster-3 中表达水平显著更高。这些分析表明,共培养中肿瘤细胞和 CAFs 之间的相互作用诱导肿瘤细胞的表型转变,从上皮状态转变为上皮-间充质混合状态,如在 CMS4 结肠癌中观察到的那样。
然后分析在单一培养和共培养中生长的CAFs之间的表型差异。Cluster 4 从单一培养物中分离的 CAF 组成,Cluster 6 从共培养物中分离的 CAF 组成,Cluster 5 由来自单一培养物和共培养物的 CAF 组成(图2 A)。差异基因表达分析显示,Cluster 6 中多种细胞外基质基因的表达发生了变化,包括COL1A1的下调,COL4A1和COL4A的上调(图2 B)。CAFs表达了非常高水平的胶原交联酶LOX和胶原裂解酶MMP1。使用免疫荧光分析表明CAF产生的胶原蛋白-4形成了与肿瘤细胞相互作用的基底膜状网状结构(图4 C)。此外,与单培养相比,共培养CAFs中反映缺氧和缺氧诱导因子1-α靶点的基因集显著更高(图2 D),进一步的分析表明,与肿瘤细胞共培养诱导了 CAF 代谢的重大转变,参与糖酵解的基因表达增加(图2 E),免疫荧光分析表明共培养CAFs中LDHA和 GAPDH 的表达显著升高(图2 F、G)。这些数据说明,共培养的 CAFs 获得缺氧、糖酵解和基质重塑表型。
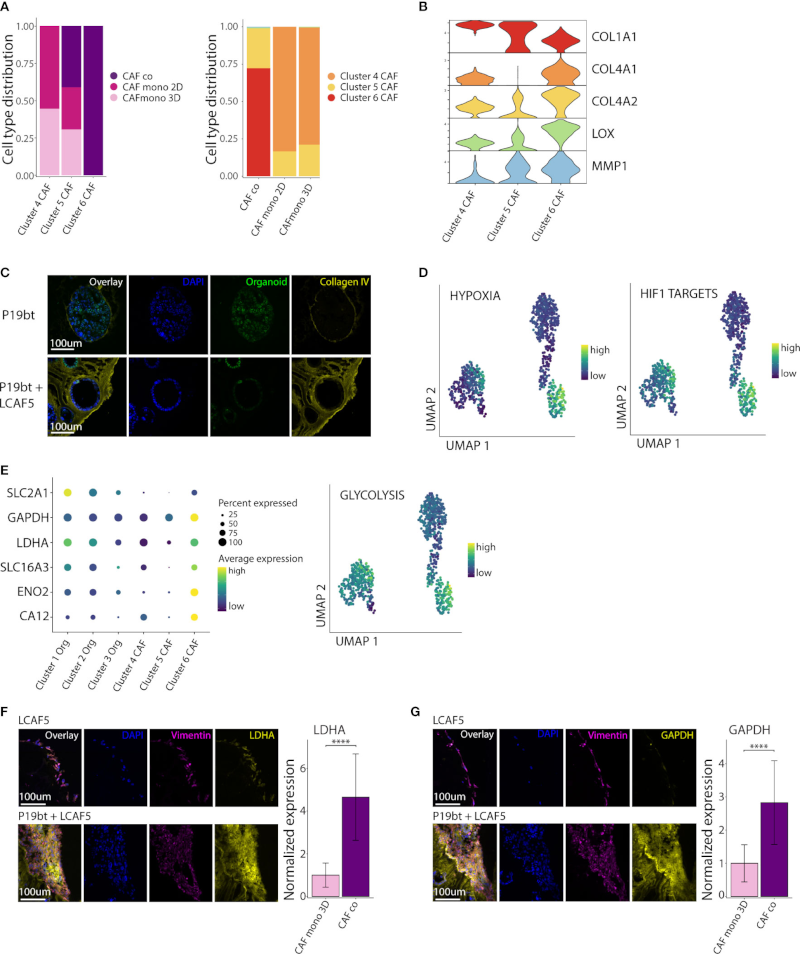
图2 共培养的 CAFs 获得缺氧、糖酵解和基质重塑表型。
目前根据转录组学特征和结直肠癌细胞的异质性对结直肠癌进行分型,定义了四种不同的结直肠癌亚型(CMS1-CMS4)。为了研究单一培养和共培养中的 CAF 表型是否与人类结肠癌中发现的 CAF 表型相似,实验利用了来自 29 名患者的原发性结肠肿瘤的大型单细胞 RNA 序列数据集。数据表明,共培养中的 CAFs 类似于在人类CMS1和CMS4结肠癌中富集的具有缺氧糖酵解表型的CAFs亚群。
上述共培养的几个特征先前与癌症中的免疫抑制有关,包括ECM硬化,缺氧和糖酵解代谢。基因表达分析显示,共培养(Cluster-6)中的CAFs表达非常高水平的免疫抑制基因,包括CXCL8、PTGS2、TGFB1和VEGFA (图3 A)。对单一培养或共培养条件培养基的分析表明,共培养比单一培养通常分泌更高水平的TGFβ1(图3 B)、VEGFA (图3 C)和乳酸(图 3 D、E),这表明产生了潜在的免疫抑制环境。
实验发现与不同CAF系共培养的细胞中分泌因子的数量存在差异,例如CR16CAF比LCAF5分泌更高水平的TGFB1,这反映了CAFs的异质性。最后,为了直接测试免疫抑制潜力,分析了条件培养基对从四个不同供体中分离的 T 细胞活化的影响。从CAF或肿瘤细胞单培养中分离的培养基分别对T细胞增殖无抑制作用和有中等抑制作用。相比之下,从 CAF/肿瘤细胞共培养中分离的培养基在所有四种情况下均有效抑制 T 细胞增殖(图3 F、G)。这些数据表明,CAFs和肿瘤细胞共培养引起的部分表型变化,导致了免疫抑制微环境的产生。
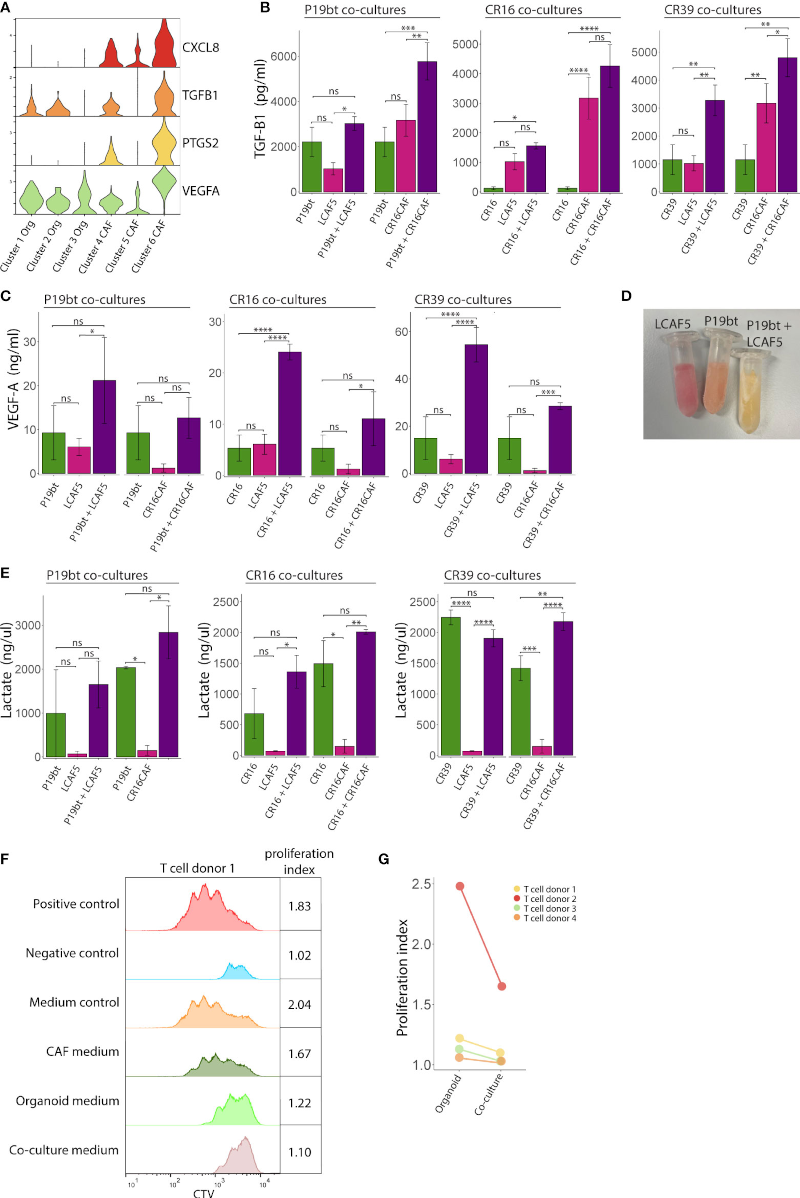
图3 共培养中免疫抑制微环境的产生。
一般来说,特异性器官微环境对远端转移的免疫环境的影响及其对免疫检查点阻断的反应是免疫肿瘤学研究的一个重要主题。该报告中开发的共培养模型系统通过合理添加特定的细胞类型和/或细胞因子和/或细胞外基质成分,可以开始对器官特异性微环境进行建模,以评估它们对T细胞行为的影响。类器官和永生化 CAFs 的共培养概括了侵袭性间充质型人结直肠癌的组织学、生理学和免疫抑制特征。该模型可用于研究免疫抑制的机制,并测试针对CAFs和肿瘤细胞之间串扰的治疗策略,也可以进一步修改以代表不同的结肠癌亚型和(器官特异性)微环境。最终,这将有助于开发涉及免疫疗法的新型联合治疗策略。
参考文献:Strating E, Verhagen MP, Wensink E, Dünnebach E, Wijler L, Aranguren I, De la Cruz AS, Peters NA, Hageman JH, van der Net MMC, van Schelven S, Laoukili J, Fodde R, Roodhart J, Nierkens S, Snippert H, Gloerich M, Rinkes IB, Elias SG, Kranenburg O. Co-cultures of colon cancer cells and cancer-associated fibroblasts recapitulate the aggressive features of mesenchymal-like colon cancer. Front Immunol. 2023 May 16;14:1053920. doi: 10.3389/fimmu.2023.1053920. PMID: 37261365; PMCID: PMC10228738.
原文链接:https://pubmed.ncbi.nlm.nih.gov/37261365/
小编旨在分享、学习、交流生物科学等领域的研究进展。如有侵权或引文不当请联系小编修正。如有任何的想法以及建议,欢迎联系小编。感谢各位的浏览以及关注!
微信搜索公众号“Naturethink”,了解更多细胞体外仿生培养技术及应用。
点击了解
细胞流体剪切力|共培养|压力培养|牵张应变|血管培养|平行平板流动腔|仪器|上海泉众机电科技有限公司Naturethink
http://www.naturethink.com/
Naturethink多细胞培养|共培养体系|共培养模型|共培养实验|动态细胞共培养|仿血流多细胞动态共培养系统
http://www.naturethink.com/?product/81.html