建立共培养血脑屏障模型以了解其对血脑屏障完整性的影响
大脑的稳态由一种称为血脑屏障(BBB)的特殊结构维持。BBB 是一种复杂的三维结构,由脑微血管内皮细胞、星形胶质细胞和周细胞组成。星形胶质细胞突起末端形成膨大的终足,包围着内皮细胞,被认为有助于维持血脑屏障。这种复合物的屏障性质由特化的脑内皮细胞维持,形成紧密的连接复合体,包括紧密连接和粘附连接。
BBB 的正常功能对于中枢神经系统(CNS)的正常和调节功能至关重要。多项研究表明,BBB 的破坏与阿尔茨海默病(AD)的发生有关。此外,神经炎症已被证明会损害 BBB 并导致 AD 的进一步发展。已知几种外周代谢紊乱,如高血糖症、糖尿病和心血管疾病,是导致血脑屏障破坏的原因,也会对 BBB 的完整性提出挑战。
由于 BBB 在神经系统疾病和药理学研究中的关键作用,BBB 模型是必不可少的组成部分。目前,已经开发了几种 BBB 模型,从单培养模型到共培养模型到更复杂的模型,如使用动物和人类细胞类型的球体和芯片模型。复杂的模型使用细胞的 3D 组织来代表 BBB 结构,并模拟脑血流。尽管有这些优点,但它们很难设置,重要的是,价格昂贵。因此,Transwell 小室共培养系统提供了一种更简单、更具成本效益和功能性的 BBB 模型。在韩国庆尚国立大学应用生命科学系、荷兰马斯特里赫特大学精神病学和神经心理学系课题组的一项研究中,描述了一种接触式共培养体外模型,使用小鼠脑内皮细胞系和星形胶质细胞系在小室培养,该系统为各种神经学研究场景提供了一个兼具高效性和功能性的平台。研究成果发表在 International Journal of Molecular Sciences 期刊题为“Establishing Co-Culture Blood-Brain Barrier Models for Different Neurodegeneration Conditions to Understand Its Effect on BBB Integrity”。

首先,将脑微血管内皮细胞系 bEnd.3 和星形胶质细胞系 C8-D1A 在小室中进行接触共培养,内皮细胞培养在顶部,而 C8-D1A 细胞接种在小室的基底外侧(图1 A-C)。粘附在膜两侧的细胞通过膜的微孔利用突出的终足显示出细胞间通讯。电子显微镜图像显示星形胶质细胞终足穿过孔膜的证据(图1 D、F)。该特性模拟了实际的 BBB,其中星形胶质细胞终足与内皮细胞接触(图1 F)。
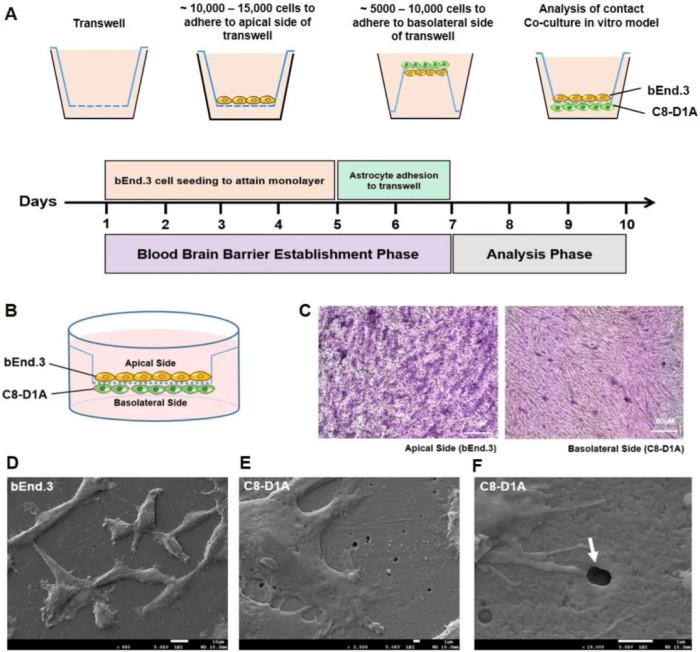
图1 建立BBB模型的体外共培养系统。
(A)时间线示意图代表bEnd.3 和 C8-D1A 细胞在小室的顶端和基底外侧接种以获得体外接触共培养 BBB 模型。(B)体外完整接触共培养BBB模型的图示。(C)苏木精和伊红(H&E)染色的transwell 膜显示在顶端和基底外侧粘附的 bEnd.3 和 C8-D1A 细胞。(D-F)扫描电子显微照片显示bEnd.3 细胞和C8-D1A 细胞,放大显微照片显示基底外侧的 C8-D1A 细胞终足穿过 0.4 μm 孔(白色箭头)到达transwell膜顶端的 bEnd.3 细胞。
在建立共培养的BBB模型后,实验检测了其屏障功能和性能。首先,分析单培养和共培养的 C8-D1A 和 bEnd.3 细胞的跨膜电阻值(TEER)值。TEER 值是膜渗透性的一个重要指标,渗透性越高 TEER 越低,它的变化能够反映膜的紧密连接功能。结果表明,共培养比单培养显示出更高的 TEER 值。此外,由于细胞的融合性,TEER 值随时间推移而增加,表明与单独培养的细胞相比,transwell 共培养显示出zui大的抗渗透性。因此,共培养的 BBB 模型可显示出有效的屏障功能和性能,说明目前的体外共培养模型可表征完整 BBB 特征。
然后,在单(不含 C8-D1A)和共(含 C8-D1A)培养模型中分析 ZO-1、occludin-1 和 caludin-5 等紧密连接蛋白的表达,以评估细胞间粘附。Western blot 分析表明,共培养模型中所有上述紧密连接蛋白的表达量都比单培养模型高 1.5-2 倍(图2 A)。此外,荧光免疫组化分析验证了这一发现,与单培养模型相比,共培养模型中的 ZO-1 表达增强(图2 B)。这说明,共培养模型显示出增强的细胞间粘附。
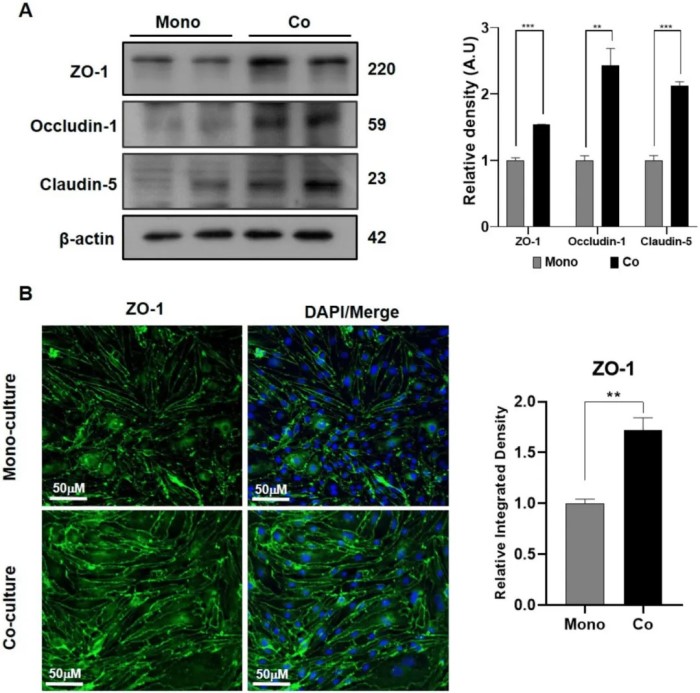
图2 共培养中脑内皮细胞表现出增强的紧密连接蛋白表达。
接下来,将 PA-BSA(牛血清白蛋白偶联棕榈酸)暴露于共培养模型 24h 来建立体外肥胖模型。免疫荧光结果显示,ZO-1水平显著下降。蛋白质印迹分析显示,紧密连接蛋白,包括 ZO-1、occludin-1 和 claudin-5 在 PA-BSA 处理的细胞中表达水平也显著下降。此外,通过测量 BBB 两端的电阻,分析了 PA-BSA 对 BBB 完整性的恶化影响。TEER 分析进一步证实了 PA-BSA 暴露显著破坏了 BBB 的电阻,从而表明 BBB 结构减弱。这说明,暴露于棕榈酸会模拟肥胖并破坏 BBB 的紧密连接。
神经炎症的特征包括负责分泌白细胞介素和细胞因子的小胶质细胞的激活。为了模拟这种情况,将共培养模型暴露于富含促炎白细胞介素和细胞因子的小胶质细胞条件培养基(MCM)。免疫荧光分析显示,与对照组相比,MCM 组的 ZO-1 表达下降,星形胶质细胞损伤标志物胶质纤维酸性蛋白(GFAP)表达显著增加(图3 A、B)。通过蛋白质印迹验证了这一发现,与未暴露的对照组相比,MCM 暴露后紧密连接蛋白的水平显著下降,而 GFAP 表达增加(图3 C、D)。
使用TEER分析了 BBB 完整性,发现暴露于 MCM 后屏障能力迅速下降(图3 E)。这说明,神经炎症影响血脑屏障通透性的下降。
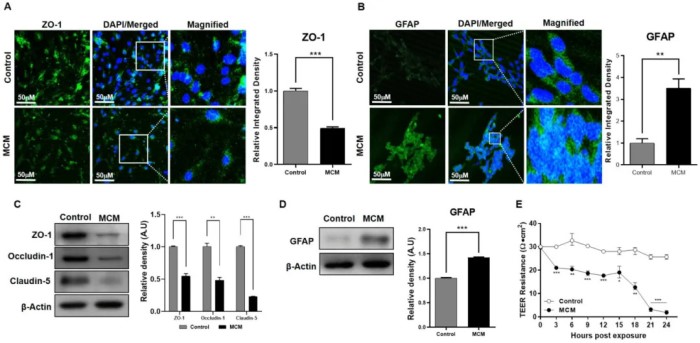
图3 促炎反应对血脑屏障的影响。
目前,普遍认为 β-淀粉样蛋白(Aβ)是构成 AD 主要病理特征,在细胞基质沉淀聚积后具有很强的神经毒性作用。研究人员使用 bEnd.3 细胞(顶部)、C8-D1A 细胞(基底膜外侧)和 HT22 细胞(下室),创建了具有三种共培养细胞系的 AD 样病理学的体外模型。HT22 细胞用淀粉样前体蛋白过表达质粒 pCAX APPswe/ind 转染或暴露于溶解在培养基中的 Aβ(1-42)多肽中进行 TEER 分析以检测 Aβ 毒性的作用。
与对照组相比,单培养模型中 ZO-1 表达水平在暴露于 Aβ 的细胞数量中显著降低(图4 A)。此外,单培养模型中的紧密连接蛋白表达水平也显著下调(图4 B)。在暴露于 Aβ 的共培养模型中,TEER 分析也显示屏障功能迅速下降(图4 C),且紧密连接蛋白表达显示出相似的下降趋势(图4 D)。Aβ 注射小鼠额叶皮层和海马区的 Western blot 分析显示,ZO-1 蛋白表达水平明显低于对照组(图4 E)。Aβ 共定位在特定的大脑区域,这证实了 Aβ 的毒性,以及在 Aβ 诱导的 AD 模型中观察到的紧密连接蛋白表达水平。这些数据表明,β淀粉样蛋白病理学导致血脑屏障破坏。
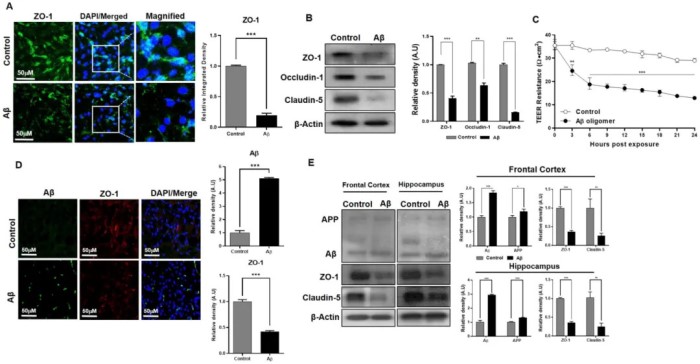
图4 淀粉样蛋白对脑内皮细胞和星形胶质细胞的毒性。
在这项研究中,开发了一种结合脑内皮细胞(bEnd.3)和星形胶质细胞(C8-D1A)的 transwell 共培养模型。总体而言,与仅内皮细胞模型(单培养)相比,共培养模型显示出更好的 BBB 结构和功能完整性,以及更高的紧密连接蛋白水平。此外,共培养模型表明,一旦暴露于上述疾病环境,其完整性和紧密连接蛋白水平就会降低。
该研究建立的体外模型,包括对物理特性、渗透性、TEER 评估和紧密连接蛋白的表达分析,而且已被用于模拟不同的大脑状况。研究人员证明,该模型是一种出色的体外血脑屏障模型,可应用于与血脑屏障完整性相关的多种疾病研究。未来,将可以作为研究复杂生理状况的便捷工具,以及治疗多种神经系统疾病的药物作用模型,如阿尔茨海默病、帕金森病、缺血、TBI和脑代谢紊乱。
参考文献:Park JS, Choe K, Khan A, Jo MH, Park HY, Kang MH, Park TJ, Kim MO. Establishing Co-Culture Blood-Brain Barrier Models for Different Neurodegeneration Conditions to Understand Its Effect on BBB Integrity. Int J Mol Sci. 2023 Mar 9;24(6):5283. doi: 10.3390/ijms24065283. PMID: 36982361; PMCID: PMC10049378.
原文链接:https://pubmed.ncbi.nlm.nih.gov/36982361/
图片来源:所有图片均来源于参考文献
本文旨在分享、交流生物领域研究进展,关注“Naturethink”公众号,了解更多相关内容。
点击了解:仿血流多细胞动态共培养系统